Sebuah bagian penting dari termodinamika adalah studi tentang transformasi antara fase yang berbeda dari suatu zat, karena proses ini terjadi dalam praktik dan sangat penting untuk memprediksi perilaku sistem dalam kondisi tertentu. Transformasi ini disebut transisi fase, yang didedikasikan untuk artikel ini.
Konsep fase dan komponen sistem

Sebelum melanjutkan ke pembahasan transisi fase dalam fisika, perlu untuk mendefinisikan konsep fase itu sendiri. Seperti diketahui dari kursus fisika umum, ada tiga keadaan materi: gas, padat dan cair. Dalam bagian khusus ilmu pengetahuan - dalam termodinamika - hukum dirumuskan untuk fase materi, dan bukan untuk keadaan agregasinya. Fasa dipahami sebagai volume materi tertentu yang memiliki struktur homogen, dicirikan oleh sifat fisik dan kimia tertentu dan dipisahkan dari materi lainnya oleh batas, yang disebut interfase.
Dengan demikian, konsep "fase" membawa informasi yang jauh lebih signifikan secara praktis tentang sifat-sifatnyapenting daripada keadaan agregasinya. Sebagai contoh, wujud padat dari logam seperti besi dapat berada dalam fase berikut: BCC non-magnetik suhu rendah, kubik berpusat muka (fcc), dan kubus berpusat muka (fcc), dan suhu tinggi. suhu bcc non-magnetik.
Selain konsep "fase", hukum termodinamika juga menggunakan istilah "komponen", yang berarti jumlah unsur kimia yang menyusun suatu sistem tertentu. Ini berarti bahwa fase dapat berupa monokomponen (1 unsur kimia) atau multikomponen (beberapa unsur kimia).
Teorema Gibbs dan kesetimbangan antara fase sistem

Untuk memahami transisi fase, perlu diketahui kondisi kesetimbangan di antara keduanya. Kondisi ini dapat diperoleh secara matematis dengan menyelesaikan sistem persamaan Gibbs untuk masing-masingnya, dengan asumsi bahwa keadaan setimbang tercapai ketika energi Gibbs total sistem yang diisolasi dari pengaruh eksternal berhenti berubah.
Sebagai hasil dari penyelesaian sistem persamaan yang ditunjukkan, diperoleh kondisi untuk adanya keseimbangan antara beberapa fase: sistem yang terisolasi akan berhenti berkembang hanya ketika tekanan, potensial kimia dari setiap komponen dan suhu di semua fase sama satu sama lain.
Aturan fase Gibbs untuk kesetimbangan

Sistem yang terdiri dari beberapa fase dan komponen tidak hanya dapat berada dalam kesetimbangandalam kondisi tertentu, misalnya pada suhu dan tekanan tertentu. Beberapa variabel dalam teorema Gibbs untuk kesetimbangan dapat diubah dengan tetap mempertahankan jumlah fase dan jumlah komponen yang berada dalam kesetimbangan ini. Banyaknya variabel yang dapat diubah tanpa mengganggu kesetimbangan dalam sistem disebut bilangan kebebasan sistem.
Jumlah kebebasan l dari sistem yang terdiri dari fase f dan komponen k ditentukan secara unik dari aturan fase Gibbs. Aturan ini secara matematis ditulis sebagai berikut: l + f=k + 2. Bagaimana cara bekerja dengan aturan ini? Sangat sederhana. Sebagai contoh, diketahui bahwa sistem terdiri dari f=3 fase kesetimbangan. Berapa jumlah minimum komponen yang dapat ditampung oleh sistem seperti itu? Anda dapat menjawab pertanyaan dengan alasan sebagai berikut: dalam kasus keseimbangan, kondisi yang paling ketat ada ketika diwujudkan hanya pada indikator tertentu, yaitu, perubahan parameter termodinamika akan menyebabkan ketidakseimbangan. Ini berarti banyaknya kebebasan l=0. Mengganti nilai l dan f yang diketahui, kita memperoleh k=1, yaitu, sistem di mana tiga fase berada dalam kesetimbangan dapat terdiri dari satu komponen. Contoh utama adalah titik tripel air, di mana es, air cair, dan uap berada dalam kesetimbangan pada suhu dan tekanan tertentu.
Klasifikasi transformasi fasa
Jika Anda mulai mengubah beberapa parameter termodinamika dalam sistem dalam kesetimbangan, Anda dapat mengamati bagaimana satu fase akan hilang dan yang lain akan muncul. Contoh sederhana dari proses ini adalah mencairnya es saat dipanaskan.
Mengingat bahwa persamaan Gibbs hanya bergantung pada dua variabel (tekanan dan suhu), dan transisi fase melibatkan perubahan pada variabel-variabel ini, maka secara matematis transisi antar fase dapat dijelaskan dengan membedakan energi Gibbs sehubungan dengannya variabel. Pendekatan inilah yang digunakan oleh fisikawan Austria Paul Ehrenfest pada tahun 1933, ketika ia menyusun klasifikasi semua proses termodinamika yang diketahui yang terjadi dengan perubahan kesetimbangan fasa.
Dari dasar termodinamika dapat disimpulkan bahwa turunan pertama energi Gibbs terhadap suhu sama dengan perubahan entropi sistem. Turunan energi Gibbs terhadap tekanan sama dengan perubahan volume. Jika, ketika fase dalam sistem berubah, entropi atau volume mengalami jeda, yaitu, mereka berubah secara tiba-tiba, maka mereka berbicara tentang transisi fase orde pertama.
Selanjutnya, turunan kedua dari energi Gibbs sehubungan dengan suhu dan tekanan masing-masing adalah kapasitas panas dan koefisien muai volumetrik. Jika transformasi antar fase disertai dengan diskontinuitas nilai kuantitas fisik yang ditunjukkan, maka orang berbicara tentang transisi fase orde dua.
Contoh transformasi antar fase

Ada banyak sekali transisi yang berbeda di alam. Dalam kerangka klasifikasi ini, contoh mencolok dari transisi jenis pertama adalah proses peleburan logam atau kondensasi uap air dari udara, ketika terjadi lonjakan volume dalam sistem.
Jika kita berbicara tentang transisi orde kedua, maka contoh yang mencolok adalah transformasi besi dari keadaan magnetis ke keadaan paramagnetik pada suhu768 C atau transformasi konduktor logam menjadi superkonduktor pada suhu mendekati nol mutlak.
Persamaan yang menjelaskan transisi jenis pertama
Dalam praktiknya, seringkali perlu diketahui bagaimana suhu, tekanan, dan energi yang diserap (dilepaskan) berubah dalam suatu sistem ketika terjadi transformasi fasa di dalamnya. Dua persamaan penting digunakan untuk tujuan ini. Mereka diperoleh berdasarkan pengetahuan tentang dasar-dasar termodinamika:
- Rumus Clapeyron, yang menetapkan hubungan antara tekanan dan suhu selama transformasi antara fase yang berbeda.
- Rumus Clausius yang menghubungkan energi yang diserap (dilepaskan) dan suhu sistem selama transformasi.
Penggunaan kedua persamaan tidak hanya untuk memperoleh ketergantungan kuantitatif besaran fisika, tetapi juga dalam menentukan tanda kemiringan kurva kesetimbangan pada diagram fasa.
Persamaan untuk mendeskripsikan transisi jenis kedua

Transisi fase jenis 1 dan 2 dijelaskan oleh persamaan yang berbeda, karena penerapan persamaan Clausius dan Clausius untuk transisi orde kedua menyebabkan ketidakpastian matematis.
Untuk menggambarkan yang terakhir, persamaan Ehrenfest digunakan, yang menetapkan hubungan antara perubahan tekanan dan suhu melalui pengetahuan tentang perubahan kapasitas panas dan koefisien ekspansi volumetrik selama proses transformasi. Persamaan Ehrenfest digunakan untuk menggambarkan transisi konduktor-superkonduktor tanpa adanya medan magnet.
Pentingdiagram fase
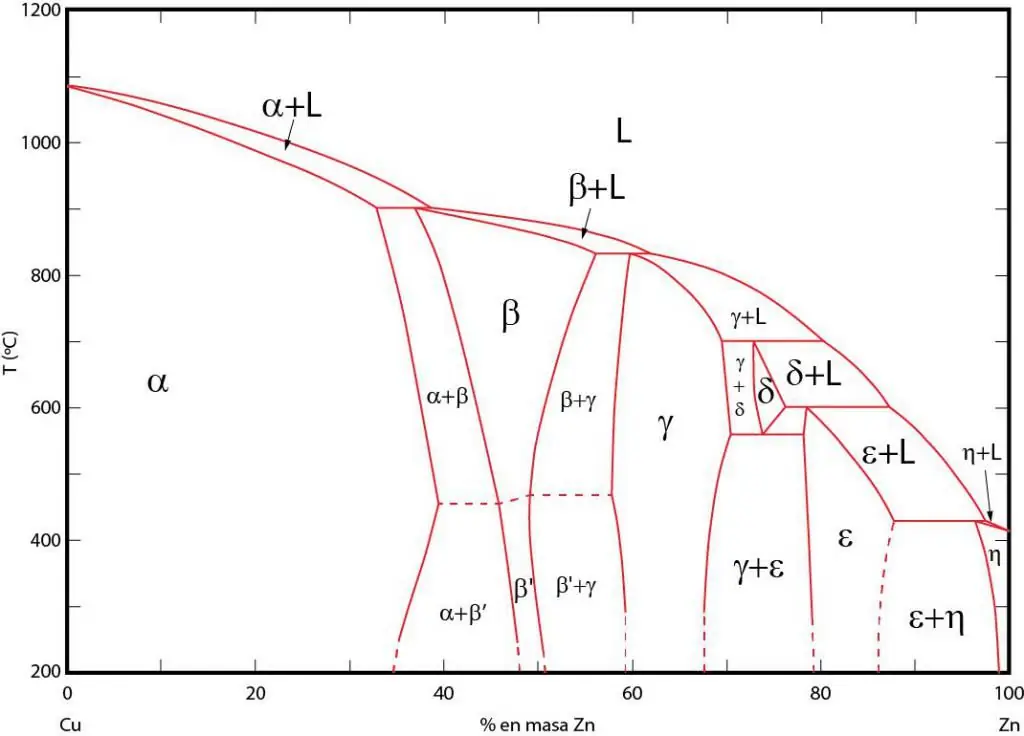
Diagram fase adalah representasi grafis dari area di mana fase yang sesuai berada dalam kesetimbangan. Daerah-daerah ini dipisahkan oleh garis kesetimbangan antara fase. Diagram fase P-T (tekanan-suhu), T-V (suhu-volume), dan P-V (volume-tekanan) sering digunakan.
Pentingnya diagram fase terletak pada kenyataan bahwa diagram fase memungkinkan Anda untuk memprediksi fase sistem saat kondisi eksternal berubah. Informasi ini digunakan dalam perlakuan panas berbagai bahan untuk mendapatkan struktur dengan sifat yang diinginkan.






