Teori kinetik-molekul memungkinkan, dengan menganalisis perilaku mikroskopis sistem dan menggunakan metode mekanika statistik, untuk memperoleh karakteristik makroskopik penting dari sistem termodinamika. Salah satu sifat mikroskopis yang berhubungan dengan suhu sistem adalah kecepatan kuadrat rata-rata molekul gas. Kami memberikan rumusnya dan mempertimbangkannya di artikel.
Gas ideal
Kami segera mencatat bahwa rumus untuk kecepatan rata-rata kuadrat molekul gas akan diberikan secara khusus untuk gas ideal. Di bawahnya, dalam fisika, sistem banyak partikel seperti itu dianggap di mana partikel (atom, molekul) tidak berinteraksi satu sama lain (energi kinetiknya melebihi energi potensial interaksi beberapa kali lipat) dan tidak memiliki dimensi, yaitu, mereka adalah titik dengan massa yang terbatas (jarak antara partikel beberapa kali lipat lebih besar dari ukurannya.linier).
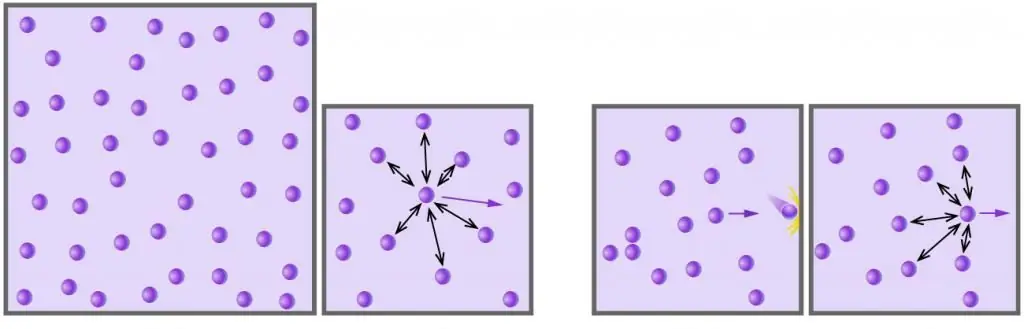
Gas apa pun yang terdiri dari molekul atau atom yang netral secara kimia, dan berada di bawah tekanan rendah serta memiliki suhu tinggi, dapat dianggap ideal. Misalnya, udara adalah gas ideal, tetapi uap air tidak lagi seperti itu (ikatan hidrogen yang kuat bekerja antara molekul air).
Teori Kinetik Molekuler (MKT)

Mempelajari gas ideal dalam kerangka MKT, Anda harus memperhatikan dua proses penting:
- Gas menciptakan tekanan dengan mentransfer ke dinding bejana yang berisi, momentum ketika molekul dan atom bertabrakan dengan mereka. Tumbukan semacam itu bersifat lenting sempurna.
- Molekul dan atom gas bergerak secara acak ke segala arah dengan kecepatan yang berbeda, distribusinya mengikuti statistik Maxwell-Boltzmann. Kemungkinan tumbukan antar partikel sangat rendah, karena ukurannya yang dapat diabaikan dan jarak yang jauh di antara mereka.
Meskipun kecepatan individu partikel gas sangat berbeda satu sama lain, nilai rata-rata dari nilai ini tetap konstan sepanjang waktu jika tidak ada pengaruh eksternal pada sistem. Rumus untuk kecepatan kuadrat rata-rata molekul gas dapat diperoleh dengan mempertimbangkan hubungan antara energi kinetik dan suhu. Kami akan membahas masalah ini di paragraf artikel berikutnya.
Derivasi dari rumus kecepatan rata-rata kuadratik molekul gas ideal
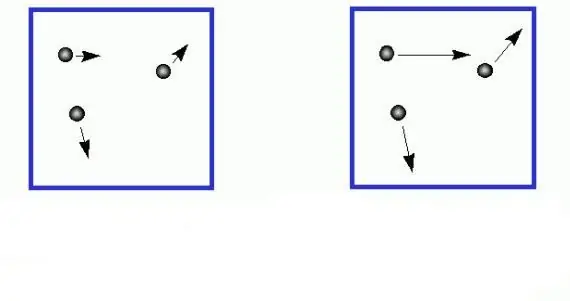
Setiap siswa mengetahui dari pelajaran fisika umum bahwa energi kinetik dari gerak translasi benda bermassa m dihitung sebagai berikut:
Ek=mv2/2
Di mana v adalah kecepatan linier. Di sisi lain, energi kinetik partikel juga dapat ditentukan dalam suhu mutlak T, menggunakan faktor konversi kB(konstanta Boltzmann). Karena ruang kita adalah tiga dimensi, Ek dihitung sebagai berikut:
Ek=3/2kBT.
Setara dengan persamaan dan menyatakan v dari keduanya, kita memperoleh rumus untuk kecepatan rata-rata gas ideal kuadrat:
mv2/2=3/2kBT=>
v=(3kBT/m).
Dalam rumus ini, m - adalah massa partikel gas. Nilainya tidak nyaman untuk digunakan dalam perhitungan praktis, karena kecil (≈ 10-27kg). Untuk menghindari ketidaknyamanan ini, mari kita ingat konstanta gas universal R dan massa molar M. Konstanta R dengan kB dihubungkan dengan persamaan:
kB=R/NA.
Nilai M didefinisikan sebagai berikut:
M=mNA.
Dengan mempertimbangkan kedua persamaan, kami memperoleh ekspresi berikut untuk kecepatan akar-rata-rata-kuadrat molekul:
v=(3RT/M).
Jadi, kecepatan kuadrat rata-rata partikel gas berbanding lurus dengan akar kuadrat suhu mutlak dan berbanding terbalik dengan akar kuadrat massa molar.
Contoh penyelesaian masalah
Semua orang tahu bahwa udara yang kita hirup adalah 99% nitrogen dan oksigen. Penting untuk menentukan perbedaan kecepatan rata-rata molekul N2 dan O2 pada suhu 15 o C.

Masalah ini akan diselesaikan secara berurutan. Pertama, kita terjemahkan suhu ke dalam satuan absolut, kita mendapatkan:
T=273, 15 + 15=288, 15 K.
Sekarang tuliskan massa molar untuk setiap molekul yang ditinjau:
MN2=0,028 kg/mol;
MO2=0,032 kg/mol.
Karena nilai massa molar sedikit berbeda, kecepatan rata-ratanya pada suhu yang sama juga harus mendekati. Menggunakan rumus untuk v, kami memperoleh nilai berikut untuk molekul nitrogen dan oksigen:
v (N2)=(38, 314288, 15/0, 028)=506,6 m/s;
v (O2)=(38, 314288, 15/0, 032)=473,9 m/s.
Karena molekul nitrogen sedikit lebih ringan daripada molekul oksigen, mereka bergerak lebih cepat. Perbedaan kecepatan rata-rata adalah:
v (N2) - v (O2)=506.6 - 473.9=32,7 m/s.
Nilai yang dihasilkan hanya 6,5% dari kecepatan rata-rata molekul nitrogen. Kami menarik perhatian pada kecepatan tinggi molekul dalam gas, bahkan pada suhu rendah.






