Transisi adiabatik antara dua keadaan dalam gas bukanlah salah satu dari proses isoproses, namun memainkan peran penting tidak hanya dalam berbagai proses teknologi, tetapi juga di alam. Pada artikel ini, kita akan membahas proses tersebut, dan juga memberikan persamaan adiabatik untuk gas ideal.
Gas ideal secara singkat
Gas ideal adalah gas yang tidak ada interaksi antar partikelnya, dan ukurannya sama dengan nol. Di alam, tentu saja, tidak ada gas ideal yang seratus persen, karena semuanya terdiri dari molekul dan atom berukuran, yang selalu berinteraksi satu sama lain setidaknya dengan bantuan gaya van der Waals. Namun demikian, model yang dijelaskan sering dilakukan dengan akurasi yang cukup untuk memecahkan masalah praktis untuk banyak gas nyata.
Persamaan utama gas ideal adalah hukum Clapeyron-Mendeleev. Itu ditulis dalam bentuk berikut:
PV=nRT.
Persamaan ini menetapkan proporsionalitas langsung antara produktekanan P pada volume V dan jumlah zat n pada suhu mutlak T. Nilai R adalah konstanta gas, yang berperan sebagai faktor proporsionalitas.
Apa yang dimaksud dengan proses adiabatik?
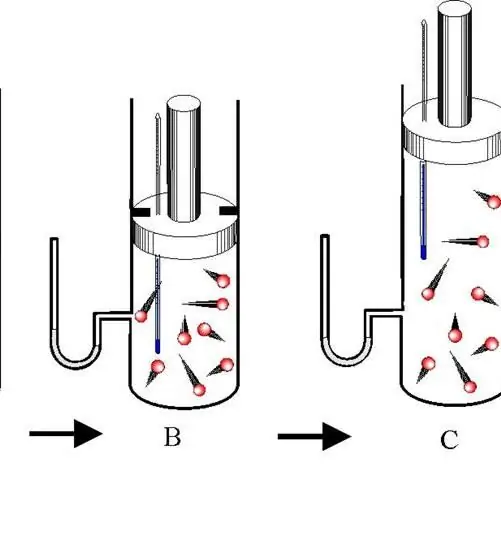
Proses adiabatik adalah transisi antara keadaan sistem gas di mana tidak ada pertukaran energi dengan lingkungan. Dalam hal ini, ketiga karakteristik termodinamika sistem (P, V, T) berubah, dan jumlah zat n tetap.
Membedakan antara ekspansi adiabatik dan kontraksi. Kedua proses terjadi hanya karena energi internal sistem. Jadi, sebagai akibat dari pemuaian, tekanan dan terutama suhu sistem turun drastis. Sebaliknya, kompresi adiabatik menghasilkan lompatan positif pada suhu dan tekanan.
Untuk mencegah pertukaran panas antara lingkungan dan sistem, sistem harus memiliki dinding berinsulasi termal. Selain itu, mempersingkat waktu proses secara signifikan mengurangi aliran panas ke dan dari sistem.
Persamaan Poisson untuk proses adiabatik

Hukum pertama termodinamika ditulis sebagai berikut:
Q=U + A.
Dengan kata lain, kalor Q yang dikomunikasikan ke sistem digunakan untuk melakukan kerja A oleh sistem dan untuk meningkatkan energi internal U. Untuk menulis persamaan adiabatik, kita harus meletakkan Q=0, yang sesuai dengan definisi proses yang sedang dipelajari. Kami mendapatkan:
ΔU=-A.
Dengan isokhorikproses dalam gas ideal, semua panas pergi untuk meningkatkan energi internal. Fakta ini memungkinkan kita untuk menulis persamaan:
ΔU=CVΔT.
Di mana CV adalah kapasitas panas isokhorik. Pekerjaan A, pada gilirannya, dihitung sebagai berikut:
A=PdV.
Di mana dV adalah perubahan volume kecil.
Selain persamaan Clapeyron-Mendeleev, persamaan berikut berlaku untuk gas ideal:
CP- CV=R.
Di mana CP adalah kapasitas panas isobarik, yang selalu lebih besar daripada kapasitas isokhorik, karena memperhitungkan kehilangan gas karena ekspansi.
Menganalisis persamaan yang ditulis di atas dan mengintegrasikan suhu dan volume, kita sampai pada persamaan adiabatik berikut:
TVγ-1=const.
Di sini adalah indeks adiabatik. Ini sama dengan rasio kapasitas panas isobarik dengan isokhorik. Persamaan ini disebut persamaan Poisson untuk proses adiabatik. Menerapkan hukum Clapeyron-Mendeleev, Anda dapat menulis dua ekspresi yang lebih mirip, hanya melalui parameter P-T dan P-V:
TPγ/(γ-1)=const;
PVγ=const.
Grafik adiabatik dapat diberikan dalam sumbu yang berbeda. Di bawah ini ditunjukkan dalam sumbu P-V.
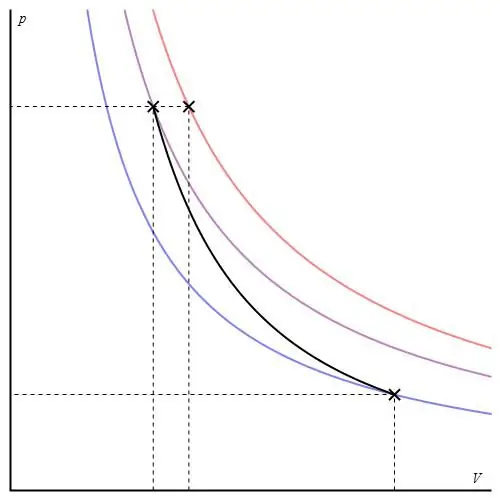
Garis berwarna pada grafik sesuai dengan isoterm, kurva hitam adalah adiabat. Seperti dapat dilihat, adiabat berperilaku lebih tajam daripada isoterm mana pun. Fakta ini mudah dijelaskan: untuk isoterm, tekanan berubah kembalisebanding dengan volume, tetapi untuk isobath, tekanan berubah lebih cepat, karena eksponennya adalah >1 untuk sistem gas apa pun.
Contoh soal
Di alam, di daerah pegunungan, ketika massa udara bergerak ke atas lereng, tekanannya turun, volumenya meningkat dan mendingin. Proses adiabatik ini menurunkan titik embun dan menghasilkan presipitasi cair dan padat.

Diusulkan untuk memecahkan masalah berikut: dalam proses mengangkat massa udara di sepanjang lereng gunung, tekanan turun 30% dibandingkan dengan tekanan di kaki. Berapa suhunya jika di kaki 25 oC?
Untuk menyelesaikan soal, gunakan persamaan adiabatik berikut:
TPγ/(γ-1)=const.
Sebaiknya ditulis dalam bentuk ini:
T2/T1=(P2/P 1)(γ-1)/γ.
Jika P1 diambil sebagai 1 atmosfer, maka P2 akan sama dengan 0,7 atmosfer. Untuk udara, indeks adiabatik adalah 1,4, karena dapat dianggap sebagai gas ideal diatomik. Nilai suhu T1 adalah 298,15 K. Substitusikan semua bilangan ini ke dalam persamaan di atas, kita dapatkan T2=269,26 K, yang sesuai dengan - 3, 9 oC.






