Gas ideal, persamaan keadaan gas ideal, suhu dan tekanannya, volumenya… daftar parameter dan definisi yang digunakan dalam bagian fisika terkait dapat dilanjutkan untuk waktu yang cukup lama. Hari ini kita akan berbicara hanya tentang topik ini.
Apa yang dipertimbangkan dalam fisika molekuler?

Objek utama yang dibahas dalam bagian ini adalah gas ideal. Persamaan keadaan gas ideal diperoleh dengan mempertimbangkan kondisi lingkungan normal, dan kita akan membicarakannya nanti. Sekarang mari kita dekati "masalah" ini dari jauh.
Katakanlah kita memiliki sejumlah massa gas. Keadaannya dapat ditentukan dengan menggunakan tiga parameter yang bersifat termodinamika. Ini, tentu saja, tekanan, volume, dan suhu. Persamaan keadaan sistem dalam hal ini akan menjadi rumus untuk hubungan antara parameter yang sesuai. Terlihat seperti ini: F (p, V, T)=0.
Di sini, untuk pertama kalinya, kita perlahan-lahan mendekati munculnya hal yang idealgas. Ini disebut gas di mana interaksi antara molekul dapat diabaikan. Secara umum, ini tidak ada di alam. Namun, setiap gas yang sangat langka dekat dengan itu. Nitrogen, oksigen, dan udara, yang dalam kondisi normal, sedikit berbeda dari ideal. Untuk menulis persamaan keadaan untuk gas ideal, kita dapat menggunakan hukum gas terpadu. Didapatkan: pV/T=const.
Konsep Terkait 1: Hukum Avogadro
Dia dapat memberi tahu kita bahwa jika kita mengambil jumlah mol yang sama dari semua gas acak dan menempatkannya dalam kondisi yang sama, termasuk suhu dan tekanan, maka gas-gas tersebut akan menempati volume yang sama. Secara khusus, percobaan dilakukan dalam kondisi normal. Ini berarti suhunya adalah 273,15 Kelvin, tekanannya adalah satu atmosfer (760 milimeter air raksa, atau 101325 Pascal). Dengan parameter ini, gas menempati volume yang sama dengan 22,4 liter. Oleh karena itu, kita dapat mengatakan bahwa untuk satu mol gas apa pun, rasio parameter numerik akan menjadi nilai konstan. Itulah sebabnya diputuskan untuk menunjuk angka ini dengan huruf R dan menyebutnya konstanta gas universal. Jadi, sama dengan 8,31 Satuannya adalah J/molK.
Gas ideal. Persamaan keadaan gas ideal dan manipulasinya
Mari kita coba menulis ulang rumusnya. Untuk melakukan ini, kami menulisnya dalam bentuk ini: pV=RT. Selanjutnya, kami melakukan tindakan sederhana, kalikan kedua sisi persamaan dengan jumlah mol yang berubah-ubah. Kami mendapatkan pVu=uRT. Mari kita memperhitungkan fakta bahwa produk dari volume molar danjumlah materi hanyalah volume. Tetapi bagaimanapun juga, jumlah mol secara bersamaan akan sama dengan hasil bagi massa dan massa molar. Seperti inilah persamaan Mendeleev-Clapeyron. Ini memberikan gambaran yang jelas tentang sistem seperti apa bentuk gas ideal. Persamaan keadaan untuk gas ideal akan berbentuk: pV=mRT/M.
Deduksi rumus untuk tekanan
Mari kita lakukan manipulasi lagi dengan ekspresi yang diperoleh. Untuk melakukannya, ruas kanan persamaan Mendeleev-Clapeyron dikalikan dan dibagi dengan bilangan Avogadro. Sekarang kita hati-hati melihat produk dari jumlah zat dengan bilangan Avogadro. Ini tidak lain adalah jumlah total molekul dalam gas. Tetapi pada saat yang sama, rasio konstanta gas universal dengan bilangan Avogadro akan sama dengan konstanta Boltzmann. Oleh karena itu, rumus untuk tekanan dapat ditulis sebagai berikut: p=NkT/V atau p=nkT. Di sini simbol n adalah konsentrasi partikel.
Proses gas ideal
Dalam fisika molekuler ada yang namanya isoproses. Ini adalah proses termodinamika yang terjadi dalam sistem pada salah satu parameter konstan. Dalam hal ini, massa zat juga harus tetap konstan. Mari kita lihat mereka lebih spesifik. Jadi, hukum gas ideal.
Tekanan tetap konstan
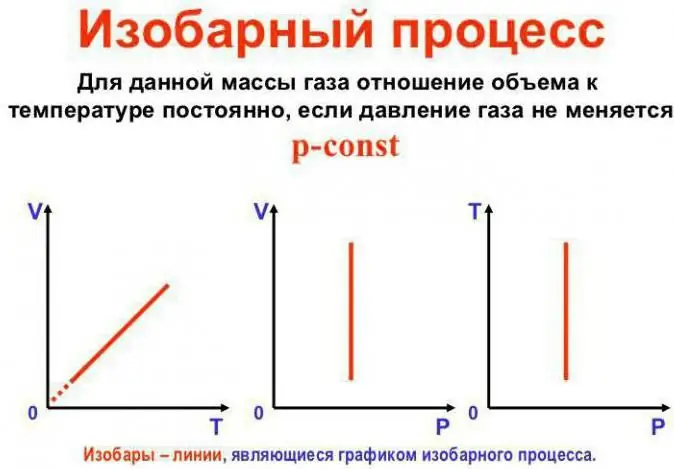
Ini adalah hukum Gay-Lussac. Terlihat seperti ini: V/T=const. Itu dapat ditulis ulang dengan cara lain: V=Vo (1 + at). Di sini a sama dengan 1/273.15 K^-1 dan disebut "koefisien muai volume". Kita dapat mengganti suhu dalam Celcius danskala Kelvin. Dalam kasus terakhir, kita mendapatkan rumus V=Voat.
Volume tetap

Ini adalah hukum kedua Gay-Lussac, lebih sering disebut sebagai hukum Charles. Terlihat seperti ini: p/T=const. Ada formulasi lain: p=po (1 + at). Transformasi dapat dilakukan sesuai dengan contoh sebelumnya. Seperti yang Anda lihat, hukum gas ideal terkadang sangat mirip satu sama lain.
Suhu tetap konstan

Jika suhu gas ideal tetap, maka kita dapat memperoleh hukum Boyle-Mariotte. Dapat ditulis seperti ini: pV=const.
Konsep Terkait 2: Tekanan Parsial
Katakanlah kita memiliki bejana berisi gas. Ini akan menjadi campuran. Sistem berada dalam keadaan kesetimbangan termal, dan gas itu sendiri tidak bereaksi satu sama lain. Di sini N akan menunjukkan jumlah total molekul. N1, N2 dan seterusnya, masing-masing, jumlah molekul di masing-masing komponen campuran. Mari kita ambil rumus tekanan p=nkT=NkT/V. Itu dapat dibuka untuk kasus tertentu. Untuk campuran dua komponen, rumusnya akan berbentuk: p=(N1 + N2) kT/V. Tetapi kemudian ternyata tekanan total akan dijumlahkan dari tekanan parsial masing-masing campuran. Jadi, itu akan terlihat seperti p1 + p2 dan seterusnya. Ini akan menjadi tekanan parsial.
Untuk apa?
Rumus yang kita peroleh menunjukkan bahwa tekanan dalam sistem berasal dari setiap kelompok molekul. Kebetulan, itu tidak tergantung padayang lain. D alton mengambil keuntungan dari ini ketika merumuskan hukum, yang kemudian dinamai menurut namanya: dalam campuran di mana gas tidak bereaksi secara kimia satu sama lain, tekanan total akan sama dengan jumlah tekanan parsial.






