Pengetahuan definisi dalam fisika merupakan faktor kunci untuk berhasil memecahkan berbagai masalah fisik. Pada artikel ini, kita akan membahas apa yang dimaksud dengan proses isobarik, isokhorik, isotermal, dan adiabatik untuk sistem gas ideal.
Gas ideal dan persamaannya
Sebelum melanjutkan ke deskripsi proses isobarik, isokhorik dan isotermal, mari kita pertimbangkan apa itu gas ideal. Di bawah definisi ini dalam fisika, mereka menganggap sistem yang terdiri dari sejumlah besar partikel tak berdimensi dan tidak berinteraksi yang bergerak dengan kecepatan tinggi ke segala arah. Faktanya, kita berbicara tentang keadaan agregat materi gas, di mana jarak antara atom dan molekul jauh melebihi ukurannya dan di mana energi potensial interaksi partikel diabaikan karena kecilnya, dibandingkan dengan energi kinetik.
Keadaan gas ideal adalah totalitas parameter termodinamikanya. Yang utama adalah suhu, volume dan tekanan. Mari kita tunjukkan masing-masing dengan huruf T, V dan P. Pada 30-an abad XIXClapeyron (seorang ilmuwan Prancis) pertama kali menuliskan persamaan yang menggabungkan parameter termodinamika yang ditunjukkan dalam persamaan tunggal. Sepertinya:
PV=nRT,
di mana n dan R masing-masing adalah jumlah zat dan konstanta gas.
Apa yang dimaksud dengan isoproses dalam gas?
Seperti yang telah diketahui banyak orang, proses isobarik, isokhorik, dan isotermal menggunakan awalan "iso" yang sama dalam namanya. Ini berarti kesetaraan satu parameter termodinamika selama perjalanan seluruh proses, sedangkan parameter lainnya berubah. Misalnya, proses isotermal menunjukkan bahwa, sebagai hasilnya, suhu absolut sistem dipertahankan konstan, sedangkan proses isokhorik menunjukkan volume konstan.
Isoproses mudah dipelajari, karena penetapan salah satu parameter termodinamika mengarah pada penyederhanaan persamaan umum keadaan gas. Penting untuk dicatat bahwa hukum gas untuk semua isoproses ini ditemukan secara eksperimental. Analisis mereka memungkinkan Clapeyron mendapatkan persamaan universal tereduksi.
Proses isobarik, isokhorik dan isotermal
Hukum pertama ditemukan untuk proses isotermal dalam gas ideal. Sekarang disebut hukum Boyle-Mariotte. Karena T tidak berubah, persamaan keadaan menyiratkan persamaan:
PV=const.
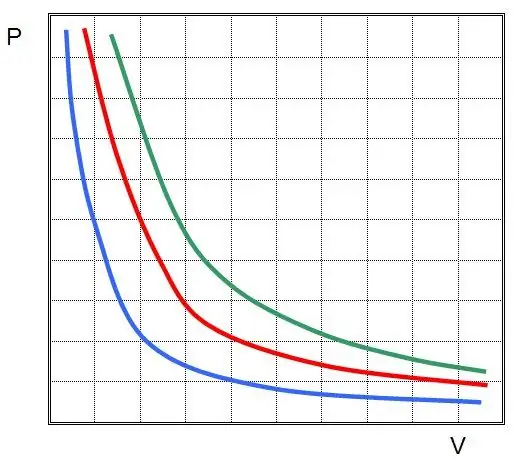
Dengan kata lain, setiap perubahan tekanan dalam sistem menyebabkan perubahan volume yang berbanding terbalik, jika suhu gas dipertahankan konstan. Grafik fungsi P(V) adalahhiperbola.
Proses Isobarik - ini adalah perubahan keadaan sistem, di mana tekanan tetap konstan. Setelah menetapkan nilai P dalam persamaan Clapeyron, kita memperoleh hukum berikut:
V/T=const.
Kesetaraan ini menyandang nama fisikawan Prancis Jacques Charles, yang menerimanya pada akhir abad ke-18. Isobar (representasi grafis dari fungsi V(T)) terlihat seperti garis lurus. Semakin banyak tekanan dalam sistem, semakin cepat garis ini naik.
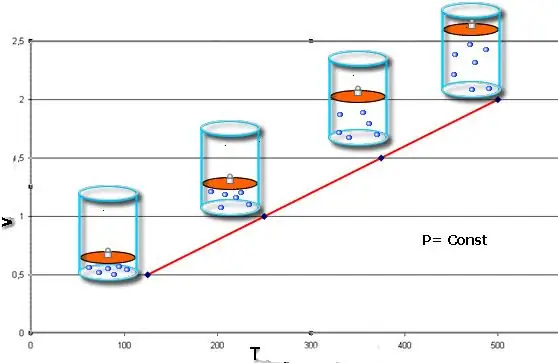
Proses isobarik mudah diterapkan jika gas dipanaskan di bawah piston. Molekul yang terakhir meningkatkan kecepatannya (energi kinetik), menciptakan tekanan yang lebih tinggi pada piston, yang mengarah pada ekspansi gas dan mempertahankan nilai konstan P.
Akhirnya, isoproses ketiga adalah isokhorik. Ini berjalan dengan volume konstan. Dari persamaan keadaan kita memperoleh persamaan yang sesuai:
P/T=const.
Hal ini dikenal di kalangan fisikawan sebagai hukum Gay-Lussac. Perbandingan langsung antara tekanan dan suhu mutlak menunjukkan bahwa grafik proses isokhorik, seperti grafik isobarik, adalah garis lurus dengan kemiringan positif.
Penting untuk dipahami bahwa semua isoproses terjadi dalam sistem tertutup, yaitu, nilai n dipertahankan selama perjalanannya.
proses adiabatik
Proses ini tidak termasuk dalam kategori "iso", karena ketiga parameter termodinamika berubah selama perjalanannya. adiabatikdisebut transisi antara dua keadaan sistem, di mana ia tidak bertukar panas dengan lingkungan. Dengan demikian, ekspansi sistem dilakukan karena cadangan energi internalnya, yang menyebabkan penurunan tekanan dan suhu absolut yang signifikan di dalamnya.
Proses adiabatik untuk gas ideal dijelaskan oleh persamaan Poisson. Salah satunya ditunjukkan di bawah ini:
PVγ=const,
di mana adalah rasio kapasitas panas pada tekanan konstan dan volume konstan.
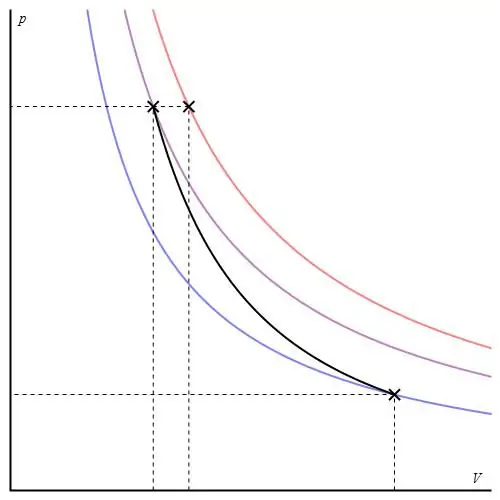
Grafik adiabatik berbeda dari grafik proses isokhorik dan grafik isobarik, tetapi mirip dengan hiperbola (isoterm). Adiabat pada sumbu P-V berperilaku lebih tajam daripada isoterm.






