Saat mempelajari perilaku gas dalam fisika, banyak perhatian diberikan pada isoproses, yaitu, transisi semacam itu antara keadaan sistem, di mana satu parameter termodinamika dipertahankan. Namun, ada transisi gas antar keadaan, yang bukan merupakan isoproses, tetapi memainkan peran penting di alam dan teknologi. Ini adalah proses adiabatik. Pada artikel ini, kita akan membahasnya secara lebih rinci, dengan fokus pada apa itu eksponen adiabatik gas.
proses adiabatik
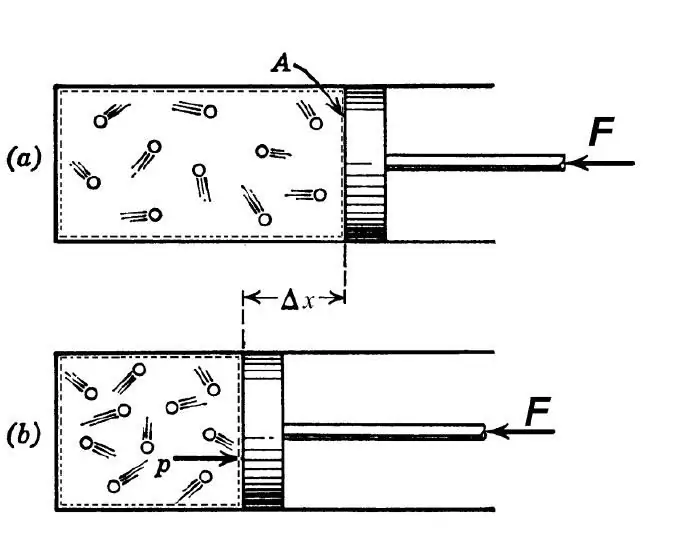
Menurut definisi termodinamika, proses adiabatik dipahami sebagai transisi antara keadaan awal dan akhir sistem, sebagai akibatnya tidak ada pertukaran panas antara lingkungan eksternal dan sistem yang dipelajari. Proses seperti itu dimungkinkan dalam dua kondisi berikut:
- konduktivitas termal antara lingkungan eksternal dansistem rendah karena satu dan lain alasan;
- kecepatan proses tinggi, sehingga pertukaran panas tidak sempat terjadi.
Dalam rekayasa, transisi adiabatik digunakan untuk memanaskan gas selama kompresi yang tajam, dan untuk mendinginkannya selama ekspansi cepat. Di alam, transisi termodinamika yang dimaksud memanifestasikan dirinya ketika massa udara naik atau turun di lereng bukit. Pasang surut tersebut menyebabkan perubahan titik embun di udara dan curah hujan.
Persamaan Poisson untuk gas ideal adiabatik

Gas ideal adalah sistem di mana partikel bergerak secara acak dengan kecepatan tinggi, tidak berinteraksi satu sama lain dan tidak berdimensi. Model seperti itu sangat sederhana dalam hal deskripsi matematisnya.
Menurut definisi proses adiabatik, persamaan berikut dapat ditulis sesuai dengan hukum pertama termodinamika:
dU=-PdV.
Dengan kata lain, gas, memuai atau mengecil, bekerja PdV karena perubahan yang sesuai dalam energi internal dU.
Dalam kasus gas ideal, jika kita menggunakan persamaan keadaan (hukum Clapeyron-Mendeleev), kita bisa mendapatkan ekspresi berikut:
PVγ=const.
Persamaan ini disebut persamaan Poisson. Orang yang akrab dengan fisika gas akan memperhatikan bahwa jika nilai sama dengan 1, maka persamaan Poisson akan masuk ke hukum Boyle-Mariotte (isotermalproses). Namun, transformasi persamaan seperti itu tidak mungkin, karena untuk semua jenis gas ideal lebih besar dari satu. Besaran (gamma) disebut indeks adiabatik dari gas ideal. Mari kita lihat lebih dekat arti fisiknya.
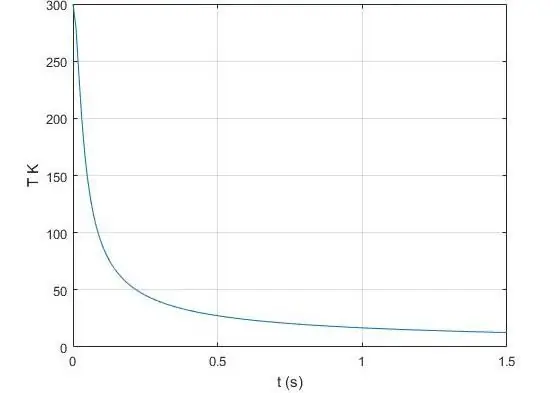
Berapa eksponen adiabatik?
Eksponen, yang muncul dalam persamaan Poisson untuk gas ideal, adalah rasio kapasitas panas pada tekanan konstan dengan nilai yang sama, tetapi sudah pada volume konstan. Dalam fisika, kapasitas kalor adalah jumlah kalor yang harus dipindahkan atau diambil dari suatu sistem agar suhunya berubah sebesar 1 Kelvin. Kami akan menyatakan kapasitas panas isobarik dengan simbol CP, dan kapasitas panas isokhorik dengan simbol CV. Maka persamaan berlaku untuk:
γ=CP/CV.
Karena selalu lebih besar dari satu, ini menunjukkan berapa kali kapasitas panas isobarik dari sistem gas yang dipelajari melebihi karakteristik isokhor yang serupa.
Kapasitas panas CP dan CV
Untuk menentukan eksponen adiabatik, seseorang harus memiliki pemahaman yang baik tentang arti besaran CP dan CV. Untuk melakukan ini, kita akan melakukan eksperimen pemikiran berikut: bayangkan gas berada dalam sistem tertutup dalam bejana dengan dinding padat. Jika bejana dipanaskan, maka semua panas yang dikomunikasikan idealnya akan diubah menjadi energi internal gas. Dalam situasi seperti itu, kesetaraan akan berlaku:
dU=CVdT.
NilaiCVmendefinisikan jumlah kalor yang harus dipindahkan ke sistem untuk memanaskannya secara isokhorik sebesar 1 K.
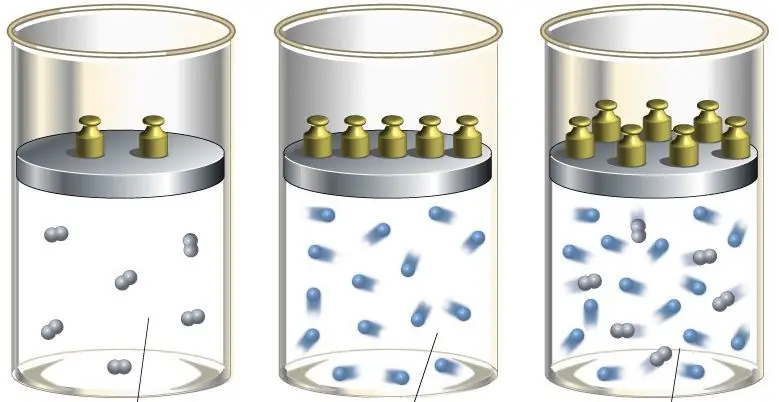
Sekarang anggaplah gas berada dalam bejana dengan piston yang bergerak. Dalam proses memanaskan sistem seperti itu, piston akan bergerak, memastikan bahwa tekanan konstan dipertahankan. Karena entalpi sistem dalam hal ini akan sama dengan produk dari kapasitas panas isobarik dan perubahan suhu, hukum pertama termodinamika akan berbentuk:
CPdT=CVdT + PdV.
Dari sini dapat dilihat bahwa CP>CV, karena dalam kasus perubahan keadaan isobarik perlu menghabiskan panas tidak hanya untuk meningkatkan suhu sistem, dan karenanya energi internalnya, tetapi juga pekerjaan yang dilakukan oleh gas selama pemuaian.
Nilai untuk gas monoatomik ideal
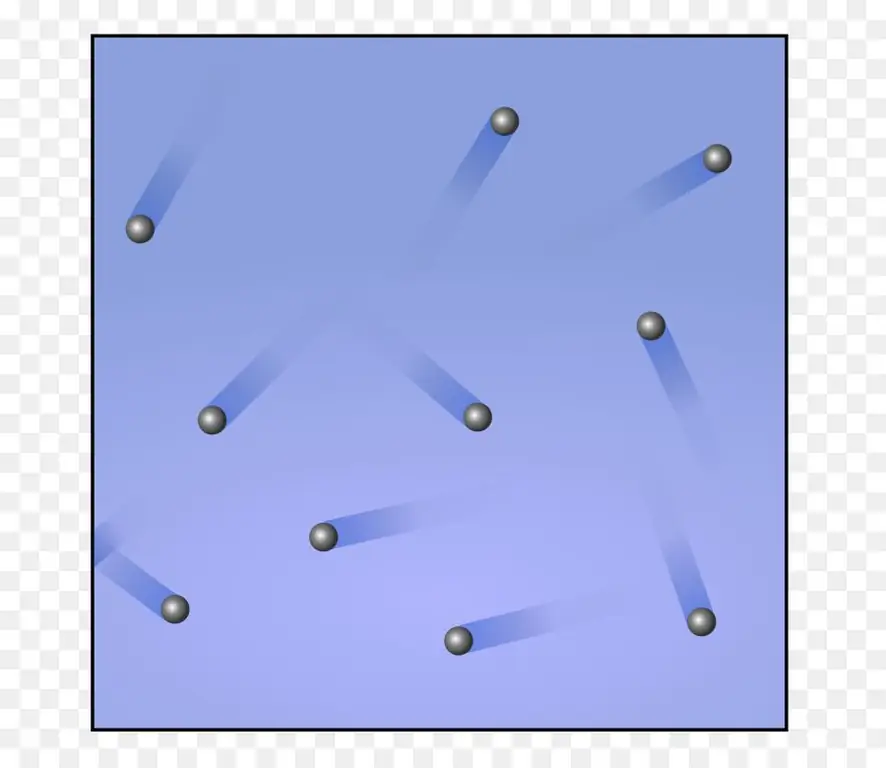
Sistem gas paling sederhana adalah gas ideal monoatomik. Misalkan kita memiliki 1 mol gas seperti itu. Ingatlah bahwa dalam proses pemanasan isobarik 1 mol gas hanya dengan 1 Kelvin, ia bekerja sama dengan R. Simbol ini biasanya digunakan untuk menunjukkan konstanta gas universal. Itu sama dengan 8, 314 J / (molK). Menerapkan ekspresi terakhir di paragraf sebelumnya untuk kasus ini, kita mendapatkan persamaan berikut:
CP=CV+ R.
Dari mana Anda dapat menentukan nilai kapasitas panas isokhorik CV:
γ=CP/CV;
CV=R/(γ-1).
Diketahui bahwa untuk satu tahi lalatgas monoatomik, nilai kapasitas panas isokhorik adalah:
CV=3/2R.
Dari dua persamaan terakhir mengikuti nilai eksponen adiabatik:
3/2R=R/(γ-1)=>
γ=5/3 1, 67.
Perhatikan bahwa nilai hanya bergantung pada sifat internal gas itu sendiri (pada sifat poliatomik molekulnya) dan tidak bergantung pada jumlah zat dalam sistem.
Ketergantungan pada jumlah derajat kebebasan
Persamaan untuk kapasitas panas isokhorik gas monoatomik ditulis di atas. Koefisien 3/2 yang muncul di dalamnya terkait dengan jumlah derajat kebebasan dalam satu atom. Ia memiliki kemampuan untuk bergerak hanya di salah satu dari tiga arah ruang, yaitu, hanya ada derajat kebebasan translasi.
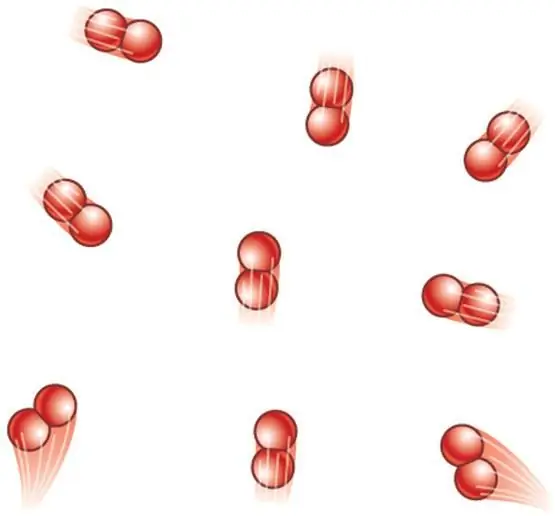
Jika sistem dibentuk oleh molekul diatomik, maka tiga derajat rotasi ditambahkan ke tiga derajat translasi. Oleh karena itu, ekspresi untuk CV menjadi:
CV=5/2R.
Maka nilai menjadi:
γ=7/5=1, 4.
Perhatikan bahwa molekul diatomik sebenarnya memiliki satu derajat kebebasan vibrasi lagi, tetapi pada suhu beberapa ratus Kelvin tidak diaktifkan dan tidak berkontribusi pada kapasitas panas.
Jika molekul gas terdiri dari lebih dari dua atom, maka mereka akan memiliki 6 derajat kebebasan. Eksponen adiabatik dalam hal ini akan sama dengan:
γ=4/3 1, 33.
JadiJadi, dengan bertambahnya jumlah atom dalam molekul gas, nilai berkurang. Jika Anda membuat grafik adiabatik pada sumbu P-V, Anda akan melihat bahwa kurva untuk gas monoatomik akan berperilaku lebih tajam daripada untuk poliatomik.
Eksponen adiabatik untuk campuran gas
Kami telah menunjukkan di atas bahwa nilai tidak bergantung pada komposisi kimia sistem gas. Namun, itu tergantung pada jumlah atom yang membentuk molekulnya. Mari kita asumsikan bahwa sistem terdiri dari N komponen. Fraksi atom komponen i dalam campuran adalah ai. Kemudian, untuk menentukan eksponen adiabatik dari campuran, Anda dapat menggunakan ekspresi berikut:
γ=i=1N(aiγ i).
Di mana i adalah nilai untuk komponen ke-i.
Misalnya, ekspresi ini dapat digunakan untuk menentukan udara. Karena terdiri dari 99% molekul diatomik oksigen dan nitrogen, indeks adiabatiknya harus sangat dekat dengan nilai 1,4, yang dikonfirmasi oleh penentuan eksperimental nilai ini.






