Kapasitas panas suatu gas adalah jumlah energi yang diserap suatu benda ketika dipanaskan satu derajat. Mari kita analisis sifat-sifat utama besaran fisis ini.

Definisi
Panas jenis gas adalah satuan massa zat tertentu. Satuan pengukurannya adalah J/(kg·K). Jumlah panas yang diserap oleh tubuh dalam proses perubahan keadaan agregasinya dikaitkan tidak hanya dengan keadaan awal dan akhir, tetapi juga dengan metode transisi.

Departemen
Kapasitas panas gas dibagi dengan nilai yang ditentukan pada volume konstan (Cv), tekanan konstan (Cр).
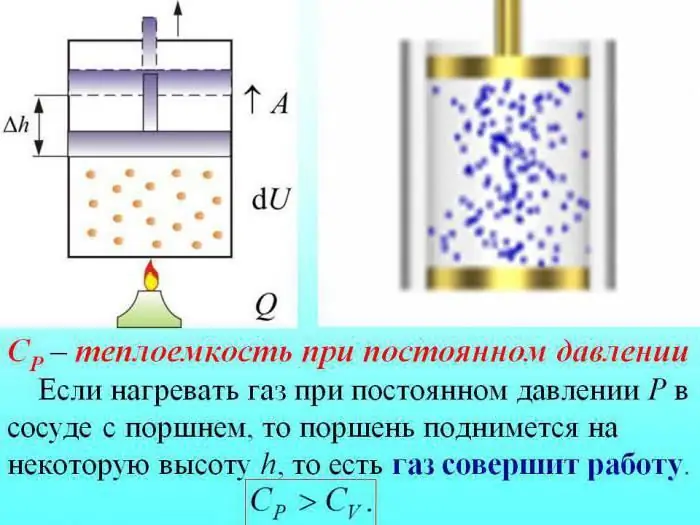
Dalam kasus pemanasan tanpa mengubah tekanan, sebagian panas dikeluarkan untuk menghasilkan kerja ekspansi gas, dan sebagian energi dihabiskan untuk meningkatkan energi internal.
Kapasitas panas gas pada tekanan konstan ditentukan oleh jumlah panas yang dihabiskan untuk meningkatkan energi internal.
Keadaan gas: fitur, deskripsi
Kapasitas panas gas ideal ditentukan dengan mempertimbangkan fakta bahwa p-Сv=R. Kuantitas terakhir disebut konstanta gas universal. Nilainya sesuai dengan 8,314 J/(mol K).
Saat melakukan perhitungan teoritis kapasitas panas, misalnya, menggambarkan hubungan dengan suhu, tidak cukup hanya menggunakan metode termodinamika, penting untuk mempersenjatai diri dengan elemen fisika statis.
Kapasitas panas gas melibatkan perhitungan nilai rata-rata energi gerak translasi beberapa molekul. Gerakan tersebut disimpulkan dari gerakan rotasi dan translasi molekul, serta dari getaran internal atom.
Dalam fisika statis, ada informasi bahwa untuk setiap derajat kebebasan gerak rotasi dan translasi, ada kuantitas untuk gas yang sama dengan setengah konstanta gas universal.

Fakta menarik
Partikel gas monoatomik diasumsikan memiliki tiga derajat kebebasan translasi, sehingga kalor jenis gas memiliki tiga derajat kebebasan translasi, dua rotasi, dan satu vibrasi. Hukum distribusi seragam mereka menyebabkan menyamakan panas spesifik pada volume konstan untuk R.
Selama percobaan, ditemukan bahwa kapasitas panas gas diatomik sesuai dengan nilai R. Perbedaan antara teori dan praktik dijelaskan oleh fakta bahwa kapasitas panas gas ideal dikaitkan dengan kuantum efek, oleh karena itu, ketika membuat perhitungan, penting untuk menggunakan statistik berdasarkan kuantummekanik.
Berdasarkan dasar mekanika kuantum, setiap sistem partikel yang berosilasi atau berputar, termasuk molekul gas, hanya memiliki beberapa nilai energi diskrit.
Jika energi gerak termal dalam sistem tidak cukup untuk membangkitkan osilasi frekuensi tertentu, gerakan tersebut tidak berkontribusi pada kapasitas panas total sistem.
Akibatnya, tingkat kebebasan tertentu menjadi "beku", tidak mungkin untuk menerapkan hukum ekuipartisi padanya.
Kapasitas panas gas merupakan karakteristik penting dari keadaan di mana fungsi seluruh sistem termodinamika bergantung.
Suhu di mana hukum ekuipartisi dapat diterapkan pada derajat kebebasan vibrasi atau rotasi dicirikan oleh teori kuantum, menghubungkan konstanta Planck dengan konstanta Boltzmann.

Gas diatomik
Kesenjangan antara tingkat energi rotasi gas semacam itu hanya beberapa derajat. Pengecualian adalah hidrogen, di mana nilai suhu ditentukan oleh ratusan derajat.
Itulah mengapa kapasitas panas gas pada tekanan konstan sulit dijelaskan dengan hukum distribusi seragam. Dalam statistik kuantum, ketika menentukan kapasitas panas, diperhitungkan bahwa bagian getarannya, dalam kasus penurunan suhu, dengan cepat berkurang dan mencapai nol.
Fenomena ini menjelaskan fakta bahwa pada suhu kamar praktis tidak ada bagian vibrasi dari kapasitas panas, untukgas diatomik, itu sesuai dengan konstanta R.
Kapasitas panas gas pada volume konstan dalam kasus indikator suhu rendah ditentukan menggunakan statistik kuantum. Ada prinsip Nernst, yang disebut hukum ketiga termodinamika. Berdasarkan formulasinya, kapasitas kalor molar suatu gas akan berkurang dengan penurunan suhu, cenderung ke nol.

Fitur benda padat
Jika kapasitas panas campuran gas dapat dijelaskan menggunakan statistik kuantum, maka untuk keadaan agregasi padat, gerakan termal dicirikan oleh sedikit fluktuasi partikel di dekat posisi kesetimbangan.
Setiap atom memiliki tiga derajat kebebasan vibrasi, oleh karena itu, sesuai dengan hukum ekuipartisi, kapasitas panas molar padatan dapat dihitung sebagai 3nR, dengan n adalah jumlah atom dalam molekul.
Dalam praktiknya, angka ini adalah batas di mana kapasitas panas benda padat cenderung pada suhu tinggi.
Maksimum dapat diperoleh pada suhu biasa untuk beberapa elemen, termasuk logam. Untuk n=1 hukum Dulong dan Petit terpenuhi, tetapi untuk zat kompleks agak sulit mencapai batas tersebut. Karena batas tidak dapat diperoleh secara nyata, terjadi dekomposisi atau pelelehan padatan.
Sejarah teori kuantum
Pendiri teori kuantum adalah Einstein dan Debye pada awal abad kedua puluh. Ini didasarkan pada kuantisasi gerakan osilasi atom dalamkristal. Dalam kasus indikator suhu rendah, kapasitas panas benda padat ternyata berbanding lurus dengan nilai absolut yang diambil pangkat tiga. Hubungan ini disebut hukum Debye. Sebagai kriteria yang memungkinkan untuk membedakan antara indikator suhu rendah dan tinggi, perbandingannya dengan suhu Debye diambil.
Nilai ini ditentukan oleh spektrum getaran atom dalam tubuh, oleh karena itu sangat tergantung pada fitur struktur kristalnya.
QD adalah nilai yang memiliki beberapa ratus K, tetapi, misalnya, nilainya jauh lebih tinggi dalam berlian.
Elektron konduksi memberikan kontribusi yang signifikan terhadap kapasitas panas logam. Untuk menghitungnya, statistik kuantum Fermi digunakan. Konduktivitas elektronik untuk atom logam berbanding lurus dengan suhu mutlak. Karena ini adalah nilai yang tidak signifikan, itu diperhitungkan hanya pada suhu yang cenderung nol mutlak.
Metode untuk menentukan kapasitas panas
Metode eksperimen utama adalah kalorimetri. Untuk melakukan perhitungan teoritis kapasitas panas, termodinamika statistik digunakan. Hal ini berlaku untuk gas ideal, serta untuk benda kristal, dilakukan berdasarkan data eksperimental pada struktur materi.
Metode empiris untuk menghitung kapasitas panas gas ideal didasarkan pada gagasan struktur kimia, kontribusi kelompok individu atom untuk Ср.
Untuk cairan, metode juga digunakan yang didasarkan pada penggunaan termodinamikasiklus yang memungkinkan untuk berpindah dari kapasitas panas gas ideal ke cairan melalui turunan dari suhu entalpi proses penguapan.
Dalam kasus larutan, perhitungan kapasitas panas sebagai fungsi aditif tidak diperbolehkan, karena nilai kelebihan kapasitas panas larutan pada dasarnya signifikan.
Untuk mengevaluasinya, kita memerlukan teori solusi statistik molekuler. Yang paling sulit adalah identifikasi kapasitas panas sistem heterogen dalam analisis termodinamika.

Kesimpulan
Studi tentang kapasitas panas memungkinkan Anda menghitung keseimbangan energi dari proses yang terjadi di reaktor kimia, serta di peralatan produksi kimia lainnya. Selain itu, nilai ini diperlukan untuk pemilihan jenis pendingin yang optimal.
Saat ini, penentuan eksperimental kapasitas panas zat untuk berbagai interval suhu - dari nilai rendah ke nilai tinggi - adalah opsi utama untuk menentukan karakteristik termodinamika suatu zat. Saat menghitung entropi dan entalpi suatu zat, integral kapasitas panas digunakan. Informasi tentang kapasitas panas reagen kimia dalam kisaran suhu tertentu memungkinkan Anda untuk menghitung efek termal dari proses tersebut. Informasi tentang kapasitas panas larutan memungkinkan untuk menghitung parameter termodinamikanya pada nilai suhu apa pun dalam interval yang dianalisis.
Misalnya, cairan ditandai dengan pengeluaran sebagian panas untuk mengubah nilai energi potensialmolekul yang bereaksi. Nilai ini disebut kapasitas panas "konfigurasi", yang digunakan untuk menjelaskan solusi.
Sulit untuk melakukan perhitungan matematis lengkap tanpa memperhitungkan karakteristik termodinamika suatu zat, keadaan agregasinya. Itulah sebabnya untuk cairan, gas, padatan, karakteristik seperti kapasitas panas spesifik digunakan, yang memungkinkan untuk mengkarakterisasi parameter energi suatu zat.






