Termodinamika keadaan agregat materi gas adalah cabang penting fisika yang mempelajari kesetimbangan termodinamika dan transisi kuasi-statis dalam sistem. Model utama yang menjadi dasar prediksi perilaku sistem adalah model gas ideal. Dengan penggunaannya, diperoleh persamaan Mendeleev-Clapeyron. Pertimbangkan dalam artikel.
Gas ideal
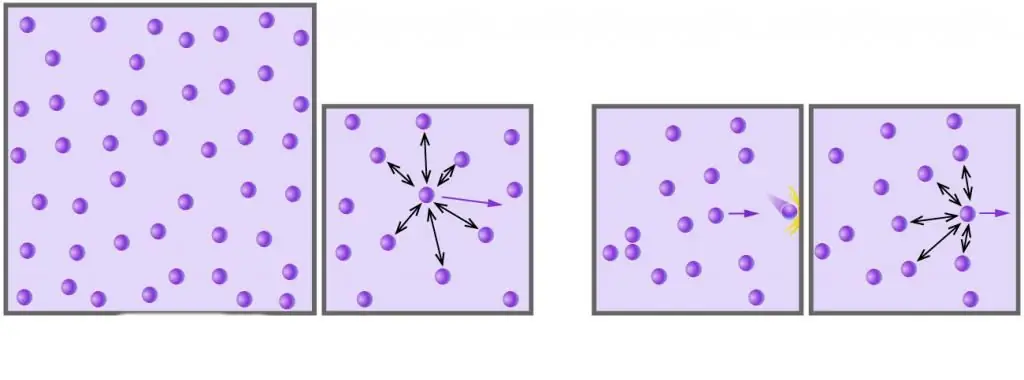
Seperti yang Anda ketahui, semua gas nyata terdiri dari molekul atau atom, yang jaraknya terlalu jauh dibandingkan dengan ukurannya pada tekanan rendah. Selain itu, pada suhu tinggi, pada skala absolut, energi kinetik molekul melebihi energi potensialnya terkait dengan interaksi dipol-dipol yang lemah (jika, selain interaksi ini, ada jenis ikatan kimia lain, misalnya, ionik atau hidrogen, maka mereka memberikan kontribusi yang signifikan terhadap komponen potensial dari energi sistem internal).
KarenaUntuk banyak gas nyata dalam kondisi mendekati normal, interaksi internal dan ukuran partikel dapat diabaikan. Kedua pendekatan utama ini merupakan model gas ideal.
Persamaan Mendeleev dalam fisika

Lebih tepat dan adil menyebut persamaan ini sebagai hukum Clapeyron-Mendeleev. Faktanya adalah bahwa itu pertama kali direkam oleh insinyur Prancis Emile Clapeyron pada tahun 1834. Dia melakukan ini dengan menganalisis hukum gas Boyle-Mariotte, Gay-Lussac dan Charles yang ditemukan pada awal abad ke-19.
Keistimewaan ahli kimia Rusia Dmitry Mendeleev terletak pada kenyataan bahwa ia memberikan persamaan bentuk matematika modern dan mudah digunakan. Secara khusus, Mendeleev memasukkan konstanta untuk semua gas ke dalam persamaan R=8, 314 J/(molK). Clapeyron sendiri menggunakan sejumlah konstanta empiris yang mempersulit proses komputasi.
Persamaan Mendeleev-Clapeyron ditulis sebagai berikut:
PV=nRT.
Kesamaan ini berarti bahwa hasil kali tekanan P dan volume V di sisi kiri ekspresi selalu sebanding dengan produk suhu mutlak T dan jumlah zat n di sisi kiri.
Ekspresi yang dipelajari memungkinkan Anda mendapatkan hukum gas apa pun jika Anda memperbaiki dua dari empat parameternya. Dalam kasus isoproses, sistem tertutup dipelajari di mana tidak ada pertukaran materi dengan lingkungan (n=konst). Proses-proses ini dicirikan oleh satu parameter termodinamika tetap (T, P atau V).

Contoh soal
Sekarang mari kita selesaikan masalah persamaan Mendeleev-Clapeyron. Diketahui oksigen seberat 500 gram berada di dalam tabung bervolume 100 liter pada tekanan 2 atmosfer. Berapa suhu dalam balon, mengingat sistem berada dalam kesetimbangan termodinamika.
Ingat bahwa, menurut definisi, jumlah suatu zat dihitung dengan rumus:
n=m/M.
Di mana m adalah massa semua partikel sistem, M adalah massa molar rata-ratanya. Persamaan ini memungkinkan kita untuk menulis ulang persamaan Mendeleev dalam bentuk berikut:
PV=mRT/M.
Di mana kita mendapatkan rumus kerja untuk tugas ini:
T=PVM/(mR).
Tinggal mengubah semua besaran menjadi satuan SI dan mensubstitusikannya ke dalam ekspresi ini:
T=21013250, 10, 032/(0, 58, 314)=156 K.
Suhu yang dihitung adalah -117 oC. Meskipun oksigen pada suhu ini masih berbentuk gas (mengembun pada -182,96 oC), dalam kondisi seperti itu model gas ideal hanya dapat digunakan untuk mendapatkan perkiraan kualitatif dari nilai yang dihitung.






