Keadaan tiga dimensi air cair sulit dipelajari, tetapi banyak yang telah dipelajari dengan menganalisis struktur kristal es. Empat atom oksigen tetangga yang berinteraksi hidrogen menempati simpul dari tetrahedron (tetra=empat, hedron=bidang). Energi rata-rata yang dibutuhkan untuk memutuskan ikatan semacam itu dalam es diperkirakan sebesar 23 kJ/mol-1.

Kemampuan molekul air untuk membentuk sejumlah rantai hidrogen, serta kekuatan tertentu, menciptakan titik leleh yang sangat tinggi. Ketika meleleh, ia ditahan oleh air cair, yang strukturnya tidak beraturan. Sebagian besar ikatan hidrogen terdistorsi. Dibutuhkan sejumlah besar energi dalam bentuk panas untuk memecahkan kisi kristal es yang terikat hidrogen.
Fitur penampakan es (Ih)
Banyak penduduk yang bertanya-tanya seperti apa kisi kristal es itu. DiperlukanPerlu dicatat bahwa kerapatan sebagian besar zat meningkat selama pembekuan, ketika pergerakan molekul melambat dan kristal padat terbentuk. Kepadatan air juga meningkat saat mendingin hingga maksimum pada 4°C (277K). Kemudian, ketika suhu turun di bawah nilai ini, ia memuai.
Peningkatan ini disebabkan oleh pembentukan kristal es ikatan hidrogen terbuka dengan kisi dan kerapatannya yang lebih rendah, di mana setiap molekul air terikat secara kaku oleh elemen di atas dan empat nilai lainnya, sambil bergerak cukup cepat untuk memiliki lebih banyak massa. Karena tindakan ini terjadi, cairan membeku dari atas ke bawah. Ini memiliki hasil biologis yang penting, sebagai akibatnya lapisan es di kolam melindungi makhluk hidup dari dingin yang ekstrem. Selain itu, dua sifat tambahan air terkait dengan karakteristik hidrogennya: panas spesifik dan penguapan.
Deskripsi detail struktur
Kriteria pertama adalah jumlah yang dibutuhkan untuk menaikkan suhu 1 gram zat sebesar 1°C. Menaikkan derajat air membutuhkan jumlah panas yang relatif besar karena setiap molekul terlibat dalam banyak ikatan hidrogen yang harus diputus agar energi kinetiknya meningkat. Omong-omong, kelimpahan H2O dalam sel dan jaringan semua organisme multiseluler besar berarti bahwa fluktuasi suhu di dalam sel diminimalkan. Fitur ini sangat penting, karena laju sebagian besar reaksi biokimiasensitif.
Panas penguapan air juga jauh lebih tinggi daripada banyak cairan lainnya. Sejumlah besar panas diperlukan untuk mengubah benda ini menjadi gas, karena ikatan hidrogen harus diputus agar molekul air terlepas satu sama lain dan memasuki fase tersebut. Benda yang dapat berubah adalah dipol permanen dan dapat berinteraksi dengan senyawa lain yang serupa dan senyawa yang terionisasi dan larut.
Zat lain yang disebutkan di atas dapat bersentuhan hanya jika ada polaritas. Senyawa inilah yang terlibat dalam struktur unsur-unsur ini. Selain itu, dapat menyelaraskan sekitar partikel-partikel yang terbentuk dari elektrolit, sehingga atom oksigen negatif dari molekul air berorientasi pada kation, dan ion positif dan atom hidrogen berorientasi pada anion.
Dalam padatan, sebagai aturan, kisi kristal molekuler dan kisi atom terbentuk. Artinya, jika yodium dibangun sedemikian rupa sehingga mengandung I2, , maka dalam karbon dioksida padat, yaitu, dalam es kering, molekul CO2 adalah terletak di node kisi kristal . Saat berinteraksi dengan zat serupa, es memiliki kisi kristal ionik. Grafit, misalnya, yang memiliki struktur atom berdasarkan karbon, tidak dapat mengubahnya, seperti halnya berlian.
Apa yang terjadi ketika kristal garam meja dilarutkan dalam air: molekul polar tertarik ke elemen bermuatan dalam kristal, yang mengarah pada pembentukan partikel serupa natrium dan klorida di permukaannya, menghasilkan benda-benda initerkilir satu sama lain, dan mulai larut. Dari sini dapat diamati bahwa es memiliki kisi kristal dengan ikatan ionik. Setiap Na + terlarut menarik ujung negatif dari beberapa molekul air, sedangkan setiap Cl - terlarut menarik ujung positif. Kulit yang mengelilingi setiap ion disebut escape sphere dan biasanya mengandung beberapa lapisan partikel pelarut.
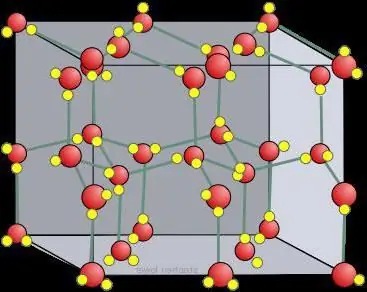
Kisi kristal es kering
Variabel atau ion yang dikelilingi oleh unsur-unsur dikatakan tersulfasi. Ketika pelarutnya adalah air, partikel-partikel tersebut terhidrasi. Jadi, setiap molekul polar cenderung dilarutkan oleh unsur-unsur benda cair. Dalam es kering, jenis kisi kristal membentuk ikatan atom dalam keadaan agregasi, yang tidak berubah. Hal lain adalah es kristal (air beku). Senyawa organik ionik seperti karboksilase dan amina terprotonasi harus larut dalam gugus hidroksil dan karbonil. Partikel yang terkandung dalam struktur seperti itu bergerak di antara molekul, dan sistem polarnya membentuk ikatan hidrogen dengan benda ini.
Tentu saja, jumlah gugus yang ditunjukkan terakhir dalam suatu molekul mempengaruhi kelarutannya, yang juga tergantung pada reaksi berbagai struktur dalam elemen: misalnya, alkohol satu-, dua- dan tiga-karbon dapat bercampur dengan air, tetapi hidrokarbon yang lebih besar dengan senyawa hidroksil tunggal jauh lebih encer dalam cairan.
Heksagonal Ih memiliki bentuk yang mirip dengankisi kristal atom. Untuk es dan semua salju alami di Bumi, tampilannya persis seperti ini. Ini dibuktikan dengan simetri kisi kristal es, yang tumbuh dari uap air (yaitu, kepingan salju). Itu berada di grup ruang P 63/mm dari 194; D 6 jam, kelas Laue 6/mm; mirip dengan -, yang memiliki kelipatan 6 sumbu heliks (rotasi sekitar selain pergeseran sepanjang itu). Ini memiliki struktur kepadatan rendah yang cukup terbuka di mana efisiensinya rendah (~1/3) dibandingkan dengan struktur kubik sederhana (~1/2) atau kubik berpusat muka (~3/4).
Dibandingkan dengan es biasa, kisi kristal es kering, terikat oleh molekul CO2, bersifat statis dan hanya berubah ketika atom meluruh.
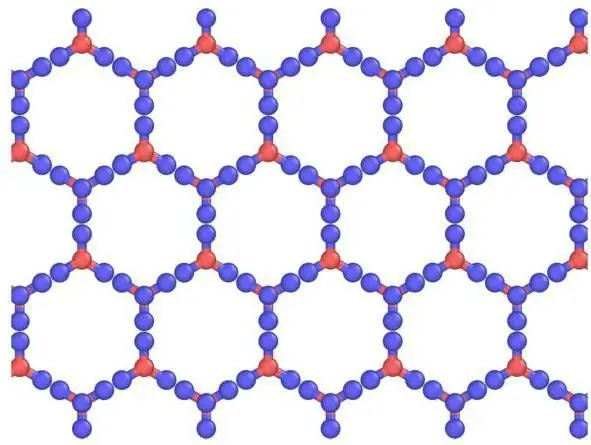
Deskripsi kisi dan elemennya
Kristal dapat dilihat sebagai model kristal, terdiri dari lembaran yang ditempatkan satu di atas yang lain. Ikatan hidrogen teratur, padahal kenyataannya acak, karena proton dapat bergerak di antara molekul air (es) pada suhu di atas sekitar 5 K. Memang, kemungkinan besar proton berperilaku seperti cairan kuantum dalam aliran terowongan yang konstan. Hal ini ditingkatkan dengan hamburan neutron, menunjukkan kepadatan hamburan mereka di tengah antara atom oksigen, menunjukkan lokalisasi dan gerakan bersama. Di sini ada kesamaan es dengan atom, kisi kristal molekul.
Molekul memiliki susunan rantai hidrogen yang terhuyung-huyungsehubungan dengan tiga tetangganya di pesawat. Unsur keempat memiliki susunan ikatan hidrogen yang terhalang. Ada sedikit penyimpangan dari simetri heksagonal sempurna, karena sel satuan 0,3% lebih pendek ke arah rantai ini. Semua molekul mengalami lingkungan molekul yang sama. Ada cukup ruang di dalam setiap "kotak" untuk menampung partikel air interstisial. Meskipun tidak dipertimbangkan secara umum, mereka baru-baru ini secara efektif dideteksi oleh difraksi neutron dari kisi kristal tepung es.
Mengubah Zat
Benda heksagonal memiliki titik rangkap tiga dengan air cair dan gas 0,01 ° C, 612 Pa, elemen padat - tiga -21,985 ° C, 209,9 MPa, sebelas dan dua -199,8 ° C, 70 MPa, serta - 34,7 ° C, 212,9 MPa. Konstanta dielektrik es heksagonal adalah 97,5.
Kurva leleh elemen ini diberikan oleh MPa. Persamaan keadaan tersedia, selain itu, beberapa ketidaksetaraan sederhana yang menghubungkan perubahan sifat fisik dengan suhu es heksagonal dan suspensi berairnya. Kekerasan berfluktuasi dengan kenaikan derajat dari atau di bawah gipsum (≦2) pada 0°C hingga feldspar (6 Mohs) pada -80°C, perubahan besar yang tidak normal dalam kekerasan absolut (> 24 kali).
Kisi kristal heksagonal es membentuk pelat dan kolom heksagonal, di mana permukaan atas dan bawah adalah bidang dasar {0 0 0 1} dengan entalpi 5,57 J cm -2, dan bagian lain yang setara disebut bagian prisma {1 0 -1 0} dengan 5, 94J cm -2. Permukaan sekunder {1 1 -2 0} dengan 6.90 J cm -2 dapat dibentuk sepanjang bidang yang dibentuk oleh sisi-sisi struktur.
Struktur seperti itu menunjukkan penurunan konduktivitas termal yang tidak wajar dengan meningkatnya tekanan (serta es kubik dan amorf dengan kepadatan rendah), tetapi berbeda dari kebanyakan kristal. Hal ini disebabkan oleh perubahan ikatan hidrogen, yang mengurangi kecepatan transversal suara dalam kisi kristal es dan air.
Ada metode yang menjelaskan cara menyiapkan sampel kristal besar dan permukaan es yang diinginkan. Diasumsikan bahwa ikatan hidrogen pada permukaan benda heksagonal yang diteliti akan lebih teratur daripada di dalam sistem curah. Spektroskopi variasi dengan pembangkitan frekuensi fase-kisi telah menunjukkan bahwa ada asimetri struktural antara dua lapisan atas (L1 dan L2) dalam rantai H2O bawah permukaan dari permukaan basal es heksagonal. Ikatan hidrogen yang diadopsi di lapisan atas segi enam (L1 O ··· HO L2) lebih kuat daripada yang diterima di lapisan kedua hingga akumulasi atas (L1 OH ··· O L2). Struktur es heksagonal interaktif tersedia.
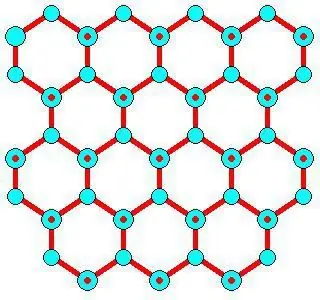
Fitur Pengembangan
Jumlah minimum molekul air yang dibutuhkan untuk membentuk es kira-kira 275 ± 25, seperti untuk gugus ikosahedral lengkap 280. Pembentukan terjadi dengan laju 10 10 pada antarmuka udara-air dan tidak dalam air curah. Pertumbuhan kristal es tergantung pada tingkat pertumbuhan yang berbeda dari berbagaienergi. Air harus dilindungi dari pembekuan ketika cryopreserving spesimen biologi, makanan dan organ.
Hal ini biasanya dicapai dengan laju pendinginan yang cepat, menggunakan sampel kecil dan cryoconservator, dan meningkatkan tekanan untuk membentuk es dan mencegah kerusakan sel. Energi bebas es/cair meningkat dari ~30 mJ/m2 pada tekanan atmosfer menjadi 40 mJ/m-2 pada 200 MPa, menunjukkan alasan mengapa efek ini terjadi.
Jenis kisi kristal apa yang menjadi ciri es
Atau, mereka dapat tumbuh lebih cepat dari permukaan prisma (S2), pada permukaan yang terganggu secara acak dari danau yang membeku atau gelisah. Pertumbuhan dari wajah {1 1 -2 0} setidaknya sama, tetapi mengubahnya menjadi alas prisma. Data tentang perkembangan kristal es telah diselidiki sepenuhnya. Tingkat pertumbuhan relatif elemen wajah yang berbeda tergantung pada kemampuan untuk membentuk tingkat hidrasi sendi yang besar. Suhu (rendah) air di sekitarnya menentukan tingkat percabangan kristal es. Pertumbuhan partikel dibatasi oleh laju difusi pada tingkat pendinginan yang rendah, yaitu <2 ° C, menghasilkan lebih banyak partikel.

Namun dibatasi oleh kinetika perkembangan pada tingkat depresi yang lebih tinggi yaitu >4°C, yang mengakibatkan pertumbuhan jarum. Bentuk ini mirip dengan struktur es kering (memiliki kisi kristal dengan struktur heksagonal), berbagaikarakteristik perkembangan permukaan dan suhu air (sangat dingin) di sekitarnya, yang berada di balik bentuk datar kepingan salju.
Pembentukan es di atmosfer sangat mempengaruhi pembentukan dan sifat awan. Feldspar, ditemukan di debu gurun yang memasuki atmosfer dalam jutaan ton per tahun, merupakan pembentuk penting. Simulasi komputer telah menunjukkan bahwa ini disebabkan oleh nukleasi bidang kristal es prismatik pada bidang permukaan berenergi tinggi.
Beberapa elemen dan kisi lainnya
Zat terlarut (dengan pengecualian helium dan hidrogen yang sangat kecil, yang dapat memasuki celah) tidak dapat dimasukkan dalam struktur Ih pada tekanan atmosfer, tetapi dipaksa keluar ke permukaan atau lapisan amorf di antara partikel tubuh mikrokristalin. Ada beberapa elemen lain di lokasi kisi es kering: ion chaotropic seperti NH4 + dan Cl -yang termasuk dalam pembekuan cair lebih ringan daripada yang kosmotropik lainnya seperti Na + dan SO42-, jadi menghilangkannya tidak mungkin karena fakta bahwa mereka membentuk lapisan tipis dari cairan yang tersisa di antara kristal. Hal ini dapat menyebabkan pengisian listrik permukaan karena disosiasi air permukaan menyeimbangkan muatan yang tersisa (yang juga dapat menyebabkan radiasi magnetik) dan perubahan pH film cairan sisa, misalnya NH 42SO4 menjadi lebih asam dan NaCl menjadi lebih basa.
Mereka tegak lurus dengan wajahkisi kristal es yang menunjukkan lapisan berikutnya yang menempel (dengan atom O berwarna hitam). Mereka dicirikan oleh permukaan basal yang tumbuh perlahan {0 0 0 1}, di mana hanya molekul air yang terisolasi yang melekat. Permukaan prisma {1 0 -1 0} yang berkembang pesat di mana pasangan partikel yang baru menempel dapat berikatan satu sama lain dengan hidrogen (satu ikatan hidrogen/dua molekul suatu unsur). Wajah yang tumbuh paling cepat adalah {1 1 -2 0} (prismatik sekunder), di mana rantai partikel yang baru menempel dapat berinteraksi satu sama lain melalui ikatan hidrogen. Salah satu molekul rantai/elemennya adalah bentuk yang membentuk punggungan yang membelah dan mendorong transformasi menjadi dua sisi prisma.
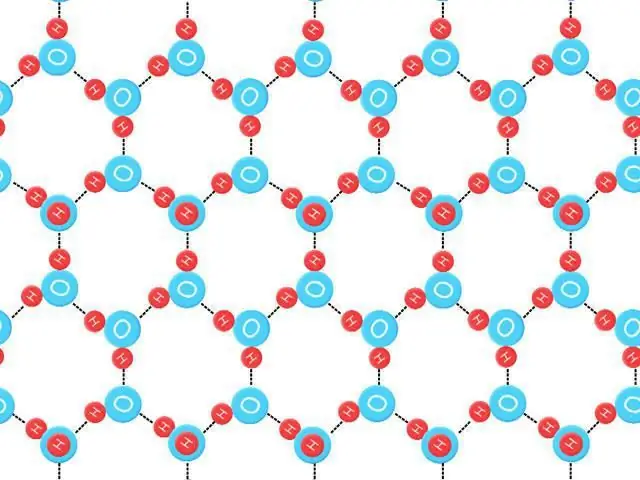
Entropi titik nol
Dapat didefinisikan sebagai S 0=k B Ln (N E0), di mana k B adalah konstanta Boltzmann, NE adalah jumlah konfigurasi pada energi E, dan E0 adalah energi terendah. Nilai entropi es heksagonal pada nol Kelvin ini tidak melanggar hukum ketiga termodinamika "Entropi kristal ideal pada nol mutlak persis nol", karena unsur dan partikel ini tidak ideal, memiliki ikatan hidrogen yang tidak teratur.
Dalam tubuh ini, ikatan hidrogen bersifat acak dan berubah dengan cepat. Struktur ini tidak persis sama dalam energi, tetapi meluas ke sejumlah besar keadaan energik dekat, mematuhi "aturan es". Entropi titik nol adalah ketidakteraturan yang akan tetap ada bahkan jika material dapat didinginkan hingga absolutnol (0 K=-273, 15 ° C). Menghasilkan kebingungan eksperimental untuk es heksagonal 3, 41 (± 0, 2) mol -1 K -1. Secara teoritis, adalah mungkin untuk menghitung entropi nol dari kristal es yang diketahui dengan akurasi yang jauh lebih tinggi (mengabaikan cacat dan penyebaran tingkat energi) daripada menentukannya secara eksperimental.
Ilmuwan dan pekerjaan mereka di bidang ini
Dapat didefinisikan sebagai S 0=k B Ln (N E0), di mana k B adalah konstanta Boltzmann, NE adalah jumlah konfigurasi pada energi E, dan E0 adalah energi terendah. Nilai entropi es heksagonal pada nol Kelvin ini tidak melanggar hukum ketiga termodinamika "Entropi kristal ideal pada nol mutlak persis nol", karena unsur dan partikel ini tidak ideal, memiliki ikatan hidrogen yang tidak teratur.
Dalam tubuh ini, ikatan hidrogen bersifat acak dan berubah dengan cepat. Struktur ini tidak persis sama dalam energi, tetapi meluas ke sejumlah besar keadaan energik dekat, mematuhi "aturan es". Entropi titik nol adalah ketidakteraturan yang akan tetap ada bahkan jika material dapat didinginkan hingga nol mutlak (0 K=-273,15 °C). Menghasilkan kebingungan eksperimental untuk es heksagonal 3, 41 (± 0, 2) mol -1 K -1. Secara teoritis, adalah mungkin untuk menghitung entropi nol dari kristal es yang diketahui dengan akurasi yang jauh lebih tinggi (mengabaikan cacat dan penyebaran tingkat energi) daripada menentukannya secara eksperimental.

Meskipun urutan proton dalam es curah tidak teratur, permukaan mungkin lebih menyukai urutan partikel-partikel ini dalam bentuk pita pasangan atom-H dan O-tunggal yang menggantung (entropi nol dengan ikatan hidrogen teratur). Ditemukan kelainan titik nol ZPE, J mol -1 K -1 dan lain-lain. Dari semua hal di atas, jelas dan dapat dimengerti jenis kisi kristal apa yang menjadi ciri es.






